Si bien se ha considerado que el hidrógeno (H2) es el combustible del futuro, aún existen muchos problemas por resolver para poder aplicarlo en forma extensiva, especialmente por su almacenamiento y elevado costo. Si bien sería deseable resolver estos problemas para evitar la emisión de dióxido de carbono (CO2) a la atmósfera, que es inevitable si se utilizan hidrocarburos como combustible y que es una de las causas principales del calentamiento global, aún serán necesarios muchos años de estudio para convertir el uso del H2 en una realidad. Sin embargo, a corto o mediano plazo esto no parece aplicable y surge, como una solución de compromiso, la necesidad de lograr un empleo más eficiente de los hidrocarburos. De esta manera, para generar la misma energía se reducirían las emisiones de CO2 y se cuidarían las reservas de estos combustibles. Esto tiene particular interés en nuestro país, que cuenta con importantes reservas de gas natural, que está fundamentalmente formado por metano (CH4). Para esto, una propuesta interesante son las celdas de combustible de óxido sólido, que pueden operar en forma directa con CH4 y otros hidrocarburos.
Las celdas de combustible son dispositivos electroquímicos que permiten la conversión de la energía de una reacción química en energía eléctrica. En el caso más sencillo, la reacción que se aprovecha es la de formación de agua a partir de H2(g) y O2(g):
H2(g) + ½ O2(g) ------> H2O(g) (1)
Para ello, separando ambos gases, se emplea un electrolito sólido (conductor iónico) que puede conducir por iones O2- o H+. Este electrolito permite el transporte de los iones de un lado al otro de la celda para producir la reacción entre ambos gases. Es importante destacar que esta forma de generación de energía prácticamente no causa contaminación y ofrece una excelente eficiencia en comparación con otros dispositivos para generación de energía.
La posibilidad de obtener energía eléctrica empleando celdas de combustible fue propuesta en 1839 por William Grove, pero las mismas dejaron de ser una curiosidad científica recién en los años '60 cuando el programa espacial de los Estados Unidos las empleó para dar energía eléctrica, calor y agua en las misiones Apollo. Se cree que en el futuro serán utilizadas en viviendas, automóviles, celulares, computadoras portátiles, etc. Desde un punto de vista teórico, las celdas de combustible son atrayentes pues podrían alcanzar altas eficiencias (energía eléctrica obtenida comparada con la entalpía de la reacción química entre los gases), del orden del 95%, en comparación con el límite de las máquinas térmicas (T2 - T1)/T2, que permite llegar sólo al 30%. En la práctica, no se han podido obtener tan altas eficiencias, alcanzándose sólo un 65% en la actualidad. Sin embargo, en los últimos años se han logrado importantes mejoras, por lo que este tema tiene un creciente interés en la comunidad científica.
Existen distintos tipos de celdas de combustible, de acuerdo con el electrolito empleado y la temperatura de operación. Las "celdas de combustible de óxido sólido" ('Solid-Oxide Fuel Cells', SOFCs), normalmente emplean electrolitos cerámicos basados en ZrO2 que conducen por anión O2- a muy alta temperatura (800-1000°C). Existen también celdas basadas en electrolitos de carbonato fundido, que conducen por iones carbonato (CO32-), que operan a aproximadamente 650°C. Es importante tener en cuenta que las celdas de menor temperatura de operación tienen menor eficiencia y requieren un procesamiento del combustible más complejo. Mientras las SOFCs pueden operar con H2, CO, CH4 u otros hidrocarburos, las PEMFCs requieren H2 de alta pureza. Por otra parte, las SOFCs tienen muy altas eficiencias, de hasta el 65%, por lo que son muy prometedoras para las aplicaciones, a pesar de la alta temperatura de operación. En este sentido, es importante tener en cuenta que, actualmente, la tendencia mundial es el estudio de SOFCs de temperatura intermedia (IT-SOFCs), que operan a temperaturas entre 500 y 700°C, gracias al empleo de nuevos materiales para electrolito y electrodo eficientes a estas temperaturas.
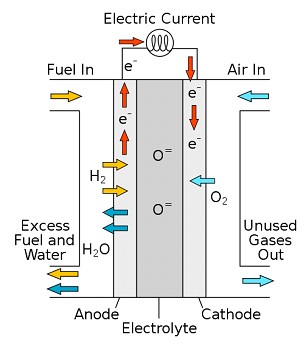
Básicamente, los procesos que tienen lugar en las SOFCs son la reducción de O2(g) a O2- en el cátodo, el transporte de iones O2- a través del electrolito sólido y la reacción de estos iones con el combustible en el ánodo. Los electrones liberados en esta última reacción, circulan nuevamente hacia el cátodo a través de un circuito externo. En la figura 1 se esquematizan los procesos que ocurren en una SOFC.